Tripelpunkt

Hermann Loring
Durch Druck undTempe-ratur eindeutig bestimmter Punkt, an dem ein Stoff gleichzeitig fest, flüssig oder gasförmig (Aggregatzustand) sein kann. DerTr. von Wasser z. B. liegt bei 610, 5 Pa (bar) und 0, 01 °C. Thermodynamik und statistische Physik, Temperatur eines Stoffes, bei der sich die drei Aggregatzustände fest, flüssig, und gasförmig im Gleichgewichtszustand befinden. Nach der Gibbsschen Phasenregel kann ein einziger Stoff nur in höchstens drei Phasen koexistieren. Die Gleichgewichtskurven festgasförmig (Sublimationskurve), gasförmigflüssig (Verdampfungskurve) und flüssigfest (Schmelzkurve) schneiden sich in einem Punkt, dem Tripelpunkt (siehe Abb.). Insbesondere ist der Tripelpunkt des Wassers ein Fixpunkt der Internationalen Temperaturskala von 1990, welcher bei 273,16 K liegt.
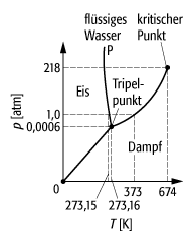
Tripelpunkt: Phasendiagramm von Wasser mit kritischem Punkt und dem Tripelpunkt, in dem sich Sublimationskurve (Verbindung 0-Tripelpunkt), Verdampfungskurve (Verbindung Tripelpunkt-kritischer Punkt) und Schmelzkurve (Verbindung Tripelpunkt-P) schneiden. Die Massstäbe sind in der Nähe des Tripelpunktes gedehnt gezeichnet.
Techniklexikon.net
Das freie Technik-Lexikon. Fundierte Informationen zu allen Fachgebieten der Ingenieurwissenschaften, für Wissenschaftler, Studenten, Praktiker & alle Interessierten. Professionell dargeboten und kostenlos zugängig.
Techniklexikon
Modernes Studium der Physik sollte allen zugängig gemacht werden.