Quantendefekt

Julian Schultheiss
Atom- und Molekülphysik, Quantenzahlverschiebung D(n, l) in Atomen mit mehreren Elektronen, die der Abschirmung der Kernladung durch innere Elektronen Rechnung trägt. Insbesondere Alkaliatome lassen sich dann analog zum Einelektronenatom beschreiben, wenn man die Hauptquantenzahl n durch die effektive Quantenzahl neff = n - D(n, l) ersetzt: Die Lage der Energieniveaus im Atom lautet dann
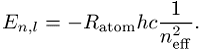
Ratom ist die Rydbergzahl (Rydberg-Konstante) des betrachteten Atoms.
Der Quantendefekt hängt in erster Ordnung von der Nebenquantenzahl l ab und ändert sich nur wenig mit steigender Hauptquantenzahl n. Er ist am stärksten für kleine l, da dann die Aufenthaltswahrscheinlichkeit des Valenzelektrons in Kernnähe (und im Einflussbereich der inneren Elektronen) am grössten ist. Der Quantendefekt ist > 1, wenn das Valenzelektron den Aufenthaltsbereich der inneren Elektronen durchdringt; er beträgt ca. 10-2, wenn nur eine Polarisation der inneren Elektronen durch die Anwesenheit des Valenzelektrons stattfindet.
Techniklexikon.net
Das freie Technik-Lexikon. Fundierte Informationen zu allen Fachgebieten der Ingenieurwissenschaften, für Wissenschaftler, Studenten, Praktiker & alle Interessierten. Professionell dargeboten und kostenlos zugängig.
Techniklexikon
Modernes Studium der Physik sollte allen zugängig gemacht werden.